1. Nêu hiện tượng, viết phương trình hóa học xảy ra khi tiến hành các thí nghiệm sau (biết
1. Nêu hiện tượng, viết phương trình hóa học xảy ra khi tiến hành các thí nghiệm sau (biết các phản ứng xảy ra hoàn roàn):
a) Cho mẩu nhỏ kim loại Na vào dung dịch AlCl3 dư.
b) Cho một vài giọt quỳ tím vào dung dịch KOH, sau đó nhỏ từ từ đến dư dung dịch H2SO4.
2. Sơn La là một tỉnh miền núi phía Bắc có nhiều núi đá vôi. Nguồn nước được sử dụng trong đời sống sinh hoạt ở Sơn La thường chứa nhiều các muối của canxi và magie (gọi là nước cứng). Bạn An lấy một mẫu nước cứng có chứa nhiều muối Ca(HCO3)2 và tiến hành các thí nghiệm sau:
Thí nghiệm 1: Đun sôi.
Thí nghiệm 2: Cho tác dụng với dung dịch Ca(OH)2.
Thí nghiệm 3: Cho tác dụng với dung dịch acid HCl.
a) Viết các phương trình phản ứng xảy ra trong các thí nghiệm trên.
b) Nước cứng gây ra nhiều tác hại trong đời sống và sản xuất như: làm giảm tác dụng của xà phòng, làm hại quần áo, làm giảm hương vị của thực phẩm khi nấu, tạo cặn trong nồi hơi gây lãng phí nhiên liệu và không an toàn...Vì vậy việc làm mềm nước cứng trước khi dùng có ý nghĩa rất quan trọng. Một trong những nguyên tắc để làm mềm nước cứng là làm giảm nồng độ các muối calcium và magnesium dưới dạng kết tủa. Vậy trong 3 thí nghiệm trên, thí nghiệm nào có thể làm mềm được mẫu nước cứng mà bạn An đã dùng? Tại sao?
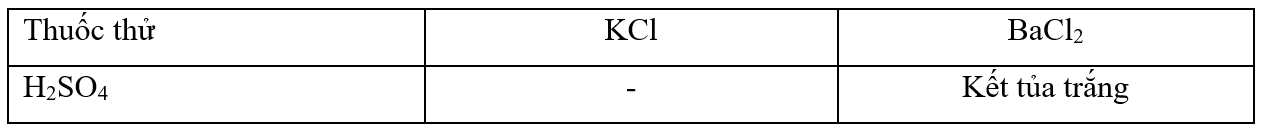
3. Có 5 dung dịch không màu riêng biệt: KCl, K2CO3, NH4Cl, NH4NO3,NH4NO3, BaCl2. Hãy trình bày cách nhận biết 5 dung dịch trên bằng phương pháp hóa học. Viết các phương trình phản ứng xảy ra.
Quảng cáo
1. Tính chất hoá học của kim loại.
2. Độ tan một số muối carbonate.
3. Tính chất hoá học của muối.
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com