1. Sulfuric acid là một hóa chất có tầm quan trọng bậc nhất trong các ngành sản xuất và đời
1. Sulfuric acid là một hóa chất có tầm quan trọng bậc nhất trong các ngành sản xuất và đời sống. Mỗi năm, thế giới cần đến hàng trăm triệu tấn sunfuric acid. Trong công nghiệp, acid sunfuric được sản xuất bằng phươg pháp tiếp xúc. Nguyên liệu là lưu huỳnh (hoặc quặng pirit sắt), Sơ đồ sản xuất sunfuric acid từ quặng pirit sắt như sau: FeS2 ⟶ SO2 ⟶ SO3 ⟶ H2SO4.
a) Nếu sử dụng 15 tấn quặng pyrite sắt (chứa 80% FeS2, còn lại là tạp chất không chứa lưu huỳnh) thì sản xuất được bao nhiêu tấn dung dịch H2SO4? Biết hiệu suất chung cho cả quá trình là 80%.
b) Trong quá trình sản xuất một lượng nhỏ SO2 bị thoát ra ngoài. Theo tiêu chuẩn quốc tế quy định, nếu lượng SO2 vượt quá $1,0.10^{- 6}~\text{mol}/\text{m}^{3}$ không khí thì bị coi là không khí ô nhiễm. Lấy 50 lít không khí ở một khu vực có nhà máy và tiến hành phân tích thấy có 0,0012 mg SO2. Hãy xác định xem khu vực nhà máy đó có bị ô nhiêm hay không?
c) Ở giai đoạn cuối cùng, lưu huỳnh trioxit được hấp thụ bằng H2SO4 đặc, tạo ra oleum (hỗn hợp các acid có công thức chung dạng $\text{H}_{2}\text{SO}_{4} \cdot \text{nSO}_{3}$ ). Sau đó pha loãng oleum vào nước thu được dung dịch acid sunfuric. Để xác định công thức của một loại oleum, tiến hành pha loãng 8,36 gam oleum vào nước thành 1,0 lít dung dịch acid sunfuric, trung hòa 1,0mL dung dịch acid này bằng dung dịch NaOH 0,1M thi thấy thể tích dung dịch NaOH cần dùng là 20mL. Xác định công thức của oleum trên.
2. Giản đồ hình bên mô tả sự biến đổi độ tan của một chất trong nước theo nhiêt độ.
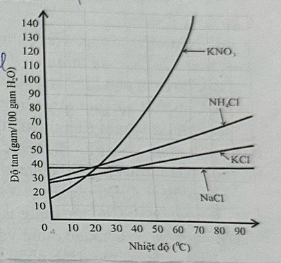
Dựa vào giản đồ hình bên hãy cho biết:
a) Chất nào có độ tan trong nước ít phụ thuộc vào nhiệt độ nhất, chất nào có độ tan trong nước thay đồi nhiều nhất theo nhiệ̣t độ?
b) Dựa vào sự khác nhau về độ tan trong nước theo nhiệt độ của NaCl và KCl hãy trình bày cách tách riêng KCl ra khỏi quặng xinvinit (NaCl.KCl) để sản xuất phân kali.
Quảng cáo
1.a. BTNT (S): FeS2 → 2H2SO4
$\left. n_{H_{2}SO_{4}} = 2.n_{FeS_{2}}\Rightarrow m_{H_{2}SO_{4}}\Rightarrow m_{dd\, H_{2}SO_{4}40\%} \right.$
Hiệu suất tổng hợp đạt 80%: $m_{dd\, H_{2}SO_{4}40\%\, tt}$(tấn)
1.b.
$m_{{so}_{2}}$ = 0,0012 mg = 0,0012.10-3 g ⟶ $n_{SO_{2}}$
Vkk = 50 lít = 50.10-3 m3
Nồng độ mol/cm3 SO2 trong khu vực nhà máy ⟹ Mức độ ô nhiếm/không ô nhiễm tại khu vực
1.c.
Để thu được 10mL dung dịch acid cần: $m_{oleum}$
H2SO4. nSO3 + nH2O → (n+1)H2SO4
Trung hoà acid:
2NaOH + H2SO4→Na2SO4 + 2H2O
$\left. M_{oleum} = \dfrac{m_{oleum}}{n}\Rightarrow n = 4 \right.$
2. Độ tan của muối
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











