S1, S2, S3 là ba hợp chất của kim loại đồng, trong đó S1, S3 là khoáng chất
S1, S2, S3 là ba hợp chất của kim loại đồng, trong đó S1, S3 là khoáng chất tự nhiên được biết đến từ lâu, có thành phần hóa học gần giống nhau. S2 có thành phần hóa học khá đơn giản nhưng kém bền, mãi tới năm 1973 người ta mới tổng hợp được hợp chất này. Cho dung dịch CuSO4 tác dụng với dung dịch Na2CO3 thu được kết tủa S1 (phản ứng 1). Nung S1 ở 500°C trong khí quyển CO2 ở áp suất rất cao (~ 20000atm ) thu được chất S2 (phản ứng 2). Trong không khí khô, S2 bị phân hủy chậm ngay ở nhiệt độ thường (phản ứng 3), còn trong không khí ẩm nó chuyển hóa thành chất S3 (phản ứng 4). Nung 1,00 gam mỗi chất S1, S2, S3 ở 300°C đến khối lượng không. Hợp chất đổi thu được m1 gam chất rắn màu đen và sản phẩm khí. Dẫn sản phẩm khí này vào dung dịch nước vôi trong dư thu được m2 gam két S2 tủa trắng. Các kết quả thí nghiệm cho trong bảng bên.
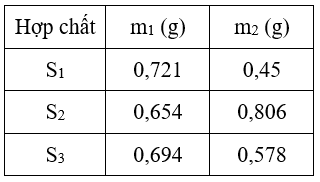
a) Xác định công thức hóa học của S1, S2, S3. Cho biết tất cả các chất đều không chứa nước kết tinh.
b) Viết phương trình hóa học của các phản ứng 1 đến 4.
Quảng cáo
a) Xác định công thức hóa học của S1, S2, S3.
Cho dung dịch CuSO4 tác dụng với dung dịch Na2CO3 thu được kết tủa S1 ⟹ S1, S2, S3 có dạng Cux(CO3)y(OH)z
+ Xét phản ứng nung S1, S2, S3: Cux(CO3)y(OH)z ⟶ CuO, CO2 và H2O.
$\left. m_{CuO}\Rightarrow n_{CuO} \right.$
Sản phẩm khí CO2 tác dụng với nược vôi trong kết tủa là CaCO3 (tương ứng m2 gam).
$n_{CO_{2}} = n_{CaCO_{3}}$
Bảo toàn khối lượng S1: $\left. m_{S_{1}} = m_{CuO} + m_{CO_{2}} + m_{H_{2}O}\Rightarrow m_{H_{2}O} \right.$
$n_{H_{2}O} = \dfrac{0,081}{18} = 0,0045(mol)$
⟹ Công thức cấu tạo S1, S2, S3
b) Viết phương trình phản ứng
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











