1. Trong công nghiệp, sulfuric acid được sản xuất từ quặng pyrite (chứa 75% FeS2 còn lại
1. Trong công nghiệp, sulfuric acid được sản xuất từ quặng pyrite (chứa 75% FeS2 còn lại là tạp chất trơ không chứa sulfur) theo sơ đồ sau:
$Fe{{S}_{2}}\xrightarrow{{}}S{{O}_{2}}\xrightarrow{{}}S{{O}_{3}}\xrightarrow{{}}{{H}_{2}}S{{O}_{4}}$
a) Viết phương trình hóa học của các phản ứng xảy ra theo sơ đồ trên.
b) Tính khối lượng dung dịch H2SO4 98% thu được từ 1 tấn quặng pyrite trên. Biết hiệu suất của quá trình sản xuất H2SO4 là 70%.
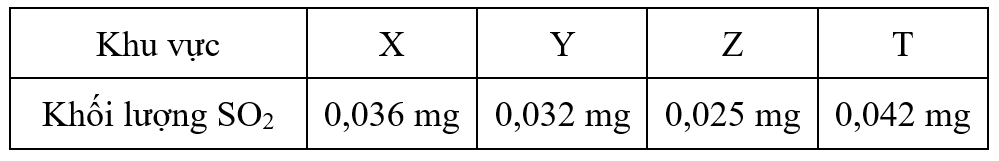
2. Khí SO2 là một trong những nguyên nhân gây ô nhiễm môi trường. Theo tiêu chuẩn quốc tế nếu nồng độ SO2 trong không khí vượt quá 10.10-6 mol/m3 thì không khí bị coi là ô nhiễm. Kết quả phân tích 50 lít không khí ở một số khu vực như sau:
a) Xác định vị trí (số thứ tự, chu kỳ, nhóm) của 2 nguyên tố S (Z = 16) và O (Z =8) trong bảng tuần hoàn các nguyên tố hoá học.
b) Trong các khu vực trên, khu vực nào không khí bị ô nhiễm? Giải thích.
Quảng cáo
1. a)Phương pháp sản xuất sulfuric acid.
b) Tính theo phương trình phản ứng.
$Fe{{S}_{2}}\xrightarrow{{}}S{{O}_{2}}\xrightarrow{{}}S{{O}_{3}}\xrightarrow{{}}{{H}_{2}}S{{O}_{4}}$
Bảo toàn nguyên tố S: $\left. n_{H_{2}SO_{4}} = 2.n_{FeS_{2}}\Rightarrow m_{H_{2}SO_{4}} \right.$
2. a) STT trong bảng tuần hoàn = Số điện tích hạt nhân của nguyên tử
STT nhóm = Số electron hoá trị
STT chu kỳ = Số lớp electron
b) Nồng độ SO2: $\dfrac{n_{SO_{2}}}{V}$
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











