1) Cho dung dịch NaOH dư lần lượt và bốn ống nghiệm đựng các dung dịch NH4Cl, Fe2(SO4)3,
1) Cho dung dịch NaOH dư lần lượt và bốn ống nghiệm đựng các dung dịch NH4Cl, Fe2(SO4)3, Ca(HCO3)2, K2SO4. Hãy viết các phương trình phản ứng hóa học xảy ra.
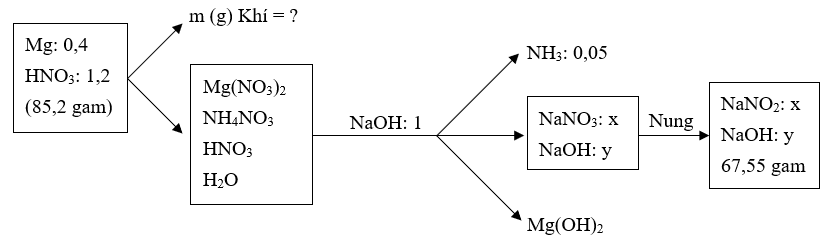
2) Cho 9,6 gam Mg tác dụng với dung dịch chứa 1,2 mol HNO3, thu được dung dịch X và m gam hỗn hợp khí. Thêm 500 ml dung dịch NaOH 2M vào X, thu được dung dịch Y, kết tủa và 1,12 lít khí Z (đktc). Lọc bỏ kết tủa, cô cạn Y thu được chất rắn T. Nung T đến khối lượng không đổi thu được 67,55 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Tìm giá trị của m.
Quảng cáo
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com