Cho cân bằng hóa học của phản ứng sau: 2NO2(g) (màu nâu đỏ) ⇌ N2O4(g)
Cho cân bằng hóa học của phản ứng sau:
2NO2(g) (màu nâu đỏ) ⇌ N2O4(g) (không màu) \(\Delta H_{298}^o\)= –58 kJ
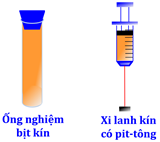
Thực hiện phản ứng trên vào trong ống nghiệm bịt kín hoặc xi lanh kín có pit-tông như hình bên.
Hãy cho biết những phát biểu sau là đúng hay sai?
| Đúng | Sai | |
|---|---|---|
| a) Khi ngâm ống nghiệm trong cốc nước đá, thấy màu khí trong ống nghiệm đậm hơn. |
||
| b) Khi đẩy pit-tông, thể tích của hệ giảm, số mol khí của hệ giảm, lúc này màu nâu đỏ nhạt dần. | ||
| c) Khi kéo pit-tông, tỉ khối của hỗn hợp khí so với không khí tăng dần. |
||
| d) Khi ngâm ống nghiệm trong cốc nước nóng, cân bằng hoá học chuyển dịch theo chiều thu nhiệt. |
Đáp án đúng là: S; Đ; S; Đ
Quảng cáo
Dựa vào nguyên lí chuyển dịch cân bằng Le Chatelier.
Đáp án cần chọn là: S; Đ; S; Đ
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com



















