1. Cho sơ đồ chuyển hóa
1. Cho sơ đồ chuyển hóa sau:
${{A}_{8}}\xleftarrow{{{H}_{2}}{{O}_{l}}}{{A}_{7}}\xleftarrow{S{{O}_{2}}(g)}{{A}_{6}}\xleftarrow{NaO{{H}_{(aq)}}}S{{O}_{2}}\xrightarrow{{{O}_{2}}_{(g)},{{V}_{2}}{{O}_{5}}}{{A}_{1}}\xrightarrow{{{H}_{2}}{{O}_{(l)}}}{{A}_{3}}$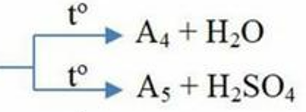
Biết: A1 đến A8 là các hợp chất của lưu huỳnh, A3 ở dạng khan, A7 chỉ chứa 3 nguyên tố hóa học.
Cho 1,330 gam A7 tác dụng với lượng dư dung dịch nước bromine, sau đó thêm lượng dư dung dịch BaCl2 tạo ra 3,262 gam kết tủa trắng không tan trong acid mạnh. Xác định công thức hóa học của A7 và viết các phương trình hóa học xảy ra của dãy chuyển hóa.
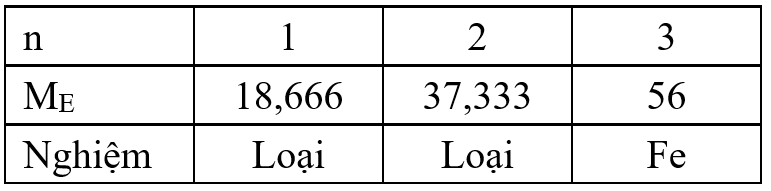
2. Nguyên tố hoá học E tạo ra hai oxide được kí hiệu là E1 và E2, trong đó phần trăm khối lượng của E trong hai oxide lần lượt là 70,00% và 72,41%.
a) Xác định nguyên tố E và công thức hoá học của E1, E2.
b) Hoà tan hoàn toàn 23,36 gam hỗn hợp G gồm E1, E2, Cu trong dung dịch HCl vừa đủ được dung dịch H. Chia H thành hai phần bằng nhau:
- Sục khí H2S dư vào phần 1 thu được 2,56 gam kết tủa.
- Thêm lượng dư dung dịch AgNO3 vào phần 2, thấy có 61,72 gam chất rắn.
Xác định khối lượng muối có trong dung dịch H, biết các phản ứng xảy ra hoàn toàn.
Quảng cáo
1. Theo giả thiết, sau khi cho A tác dụng với nước Br2 thu dung dịch rồi thêm lượng dư BaCl2 thì tạo ra 3,262 gam kết tủa trắng không tan trong acid mạnh. Vì A chứa S đồng thời Br2/H2O là chất oxi hóa mạnh nên kết tủa là BaSO4 ⟹ $n_{BaSO_{4}}$
Bảo toàn nguyên tố S: Mol S trong A7 = 0,014 (mol)
Trong A7 có một nguyên tố S ⟹ $M_{A_{7}}$
Trong A7 có hai nguyên tố S ⟹ $M_{A_{7}}$
Viết phương trình phản ứng.
2. a) Đặt công thức tổng quát của E1 và M2On và E2 là M2Om (n, m có các giá trị: 1,2,3 hoặc 8/3)
Xét E1, có $\% m_{E} = \dfrac{2M_{E}}{2M_{E} + 16n}.100\% = 70\%$
Biện luận, xác định Fe
Xét E2: %M = 72,41% ⟹ Xác định công thức hoá học của E2
b) Khối lượng muối có trong dung dịch II:
Khi hòa tan hỗn hợp Fe2O3 và Fe3O4 và Cu trong dung dịch HCl vừa đủ thu được hỗn hợp H chứa tối đa và số mol mỗi chất trong mỗi phần là CuCl2: x (mol), FeCl2: y (mol), FeCl3: z (mol).
$\left\{ \begin{array}{l} {Cu} \\ {Fe_{2}O_{3}} \\ {Fe_{3}O_{4}} \end{array} \right.\overset{+ HCl}{\rightarrow}\left\{ \begin{array}{l} {CuCl_{2}:x} \\ {FeCl_{2}:y} \\ {FeCl_{3}:z} \end{array} \right.\, + H_{2}O$
$\begin{array}{l} {BTNT(Cl):n_{HCl}} \\ {BTNT(H):2.n_{H_{2}O} = n_{HCl}} \\ {BTNT(O):n_{O(oxide)} = n_{O(H_{2}O)}} \end{array}$
Lập hệ phương trình, xác định ẩn x, y, z
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com