1. Enthalpy tạo thành chuẩn (hay nhiệt tạo thành chuẩn) của một chất ở 298K, kí
1. Enthalpy tạo thành chuẩn (hay nhiệt tạo thành chuẩn) của một chất ở 298K, kí hiệu là $\Delta_{f}H_{298}^{o}$, là nhiệt lượng kèm theo phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền nhất và phổ biến nhất của các nguyên tố có mặt trong chất, ở 1 bar và 298K.
Cho nhiệt tạo thành chuẩn của các chất như sau:
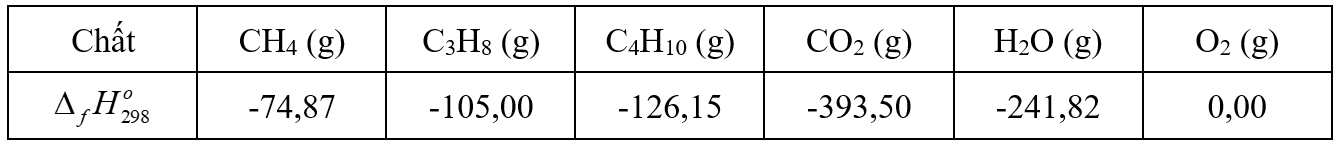
(g): trạng thái khí
Biết rằng biến thiên enthalpy chuẩn ở 298K của một phản ứng hoá học (kí hiệu là $\Delta_{r}H_{298}^{o}$) được tính bằng tổng nhiệt lượng tạo thành chuẩn $\Delta_{f}H_{298}^{o}$ của các chất sản phẩm trừ đi tổng nhiệt tạo thành chuẩn $\Delta_{f}H_{298}^{o}$ của các chất tham gia phản ứng (chú ý: có nhân hệ số của các chất trong phương trình hoá học). Khi phản ứng toả nhiệt thì $\Delta_{r}H_{298}^{o}$ < 0; khi phản ứng thu nhiệt thì $\Delta_{r}H_{298}^{o}$ > 0. Giả sử khí biogas gồm CH4 và các khí khác không cháy, còn khí gas dân dụng gồm C3H8 và C4H10 với tỉ lệ mol 1 : 1.
a) Giải thích tại sao C3H8 và C4H10 không có mùi nhưng khí gas dân dụng lại có mùi đặc trưng?
b) Để tạo thành cùng một nhiệt lượng Q, có thể đốt khí gas dân dụng hoặc khí biogas. Bằng tính toán hãy cho biết trong trường hợp đốt khí gas nào tạo ra nhiều khí CO2 hơn?
c) Giả sử một bình gas dân dụng chứa 12kg khí gas. Một hộ gia đinh cần sử dụng 10 000 kJ mỗi ngày bằng việc đốt cháy khí gas và hiệu suất sử dụng nhiệt từ phản ứng đốt cháy là 65%. Hỏi hộ gia đình có thể sử dụng bình gas trên được bao nhiêu ngày?
2. G1 là một muối carbonate trung hoà ngậm nước của một kim loại hoá trị I được tìm thấy ở những vùng khí hậu khô cằn, trên bề mặt hoặc trong các hốc núi lửa. Hoà tan 44,64 gam G1 trong 100 gam nước ở 80oC, sau đó làm lạnh xuống 20oC thu được 65,78 gam tinh thể G2 (có khối lượng mol phân tử nhỏ hơn 350 g/mol) và dung dịch K1. Khi thêm từ từ 25 mL dung dịch HCl 36% (khối lượng riêng 1,18 g/mL) vào dung dịch K1 thu được 102,64 gam dung dịch K2. Cho bay hơi đến khô dung dịch K2 thu được 15,21 gam chất rắn G3.
a) Biện luận các trường hợp có thể xảy ra trong điều kiện bài toàn để xác định công thức hoá học của G1, G2 và thành phần các chất trong G3, K1, K2.
b) Hoà tan 5,456 gam G1 vào 100 gam nước thì nhiệt độ dung dịch tăng lên 1,05 độ. Hoà tan 4,004 gam G2 vào 200 gam nước thì nhiệt độ dung dịch giảm đi 1,08 độ. Tính lượng nhiệt (quy về kJ/mol) kèm theo quá trình hoà tan G1 và G2 trong điều kiện đã cho. Giả sử nhiệt dung riêng của các dung dịch tạo thành bằng nhiệt dung riêng của nước (4,18 J/gxđộ).
Quảng cáo
1. a) Khứu giác nhạy với các khí có mùi khó chịu hơn.
b) $\Delta_{r}H_{298}^{o} = {\sum{\Delta_{f}H_{298}^{o}(sp)}} - {\sum{\Delta_{f}H_{298}^{o}(cd)}}$
CH4 + 2O2 ⟶ CO2 + 2H2O
C3H8 + 5O2 ⟶ 3CO2 + 4H2O
C4H10 + 6,5O2 ⟶ 4CO2 + 5H2O
Xác định nhiệt lượng toả ra khi đốt cháy 1 mol khí gas và 1 mol khí CH4.
So sánh số mol khí CO2 tạo thành
c) 12kg gas ⟹ số mol gas
⟹ Thời gian sử dụng
2. a) G1 có dạng M2CO3.xH2O
Khối lượng G2 tạo ra trong quá trình kết tinh G1, lớn hơn khối lượng G1 ⟹ G2 là muối ngậm nước có dạng M2CO3.yH2O (y > x)
⟹ Khối lượng dung dịch K1và thành phần dung dịch K1
$n_{HCl} = \dfrac{m_{HCl}}{M_{HCl}}$
Sự giảm khối lượng dung dịch sau khi thêm HCl là do tạo thành khí CO2 thoát ra khỏi dung dịch
⟹ mdung dịch giảm= mCO2 ⟹ $n_{CO_{2}} = \dfrac{m_{CO_{2}}}{M_{CO_{2}}}$
Cho từ từ HCl vào dung dịch M2CO3 có thể xảy ra các phản ứng:
HCl + M2CO3 ⟶ MCl + MHCO3
HCl + MHCO3 ⟶ MCl + CO2 + H2O
Trường hợp 1: HCl dư và G3 là muối MCl
Trường hợp 2: HCl hết và G3 gồm MCl, MHCO3
Biện luận xác định kim loại M
b) Nhiệt lượng toả ra/thu vào = 4,18.mdung dịch.độ:n
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











