Tốc độ phản ứng và cân bằng hóa học
Chuyên đề này giúp các em giải được các bài tập về cân bằng và sự chuyển dịch cân bằng hóa học.
Lưu ý: Chức năng này hiện không còn dùng nữa, vui lòng chọn các khóa học để xem các bài giảng hoặc làm đề thi online!
Bài tập luyện
Câu hỏi số 1:
Cho cân bằng: 2AB2 (k) + B2 (k) ⇌ 2AB3 (k). Khi tăng nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 giảm đi. Phát biểu đúng khi nói về cân bằng này là:
Câu hỏi số 2:
Trong một bình kín dung tích 10 lít nung một hỗn hợp gồm 1 mol N2 và 4 mol H2 ở nhiệt độ t0C và áp suất P. Khi phản ứng đạt đến trong thái cân bằng thu được một hỗn hợp trong đó NH3 chiếm 25% thể tích. Xác định hằng số cân bằng KC của phản ứng: N2 + 3H2 <=> 2NH3.
Câu hỏi số 3:
Cho cân bằng hoá học sau: 2NH3(k) ⇌ N2(k) + 3H2(k). Khi tăng nhiệt độ của hệ thì tỉ khối của hỗn hợp so với hiđro giảm. Nhận xét nào sau đây là đúng?
Câu hỏi số 4:
Thực hiện phản ứng trong bình kín có dung tích 500ml với 1 mol N2 , 4 mol H2 và một ít xúc tác (có thể tích không đáng kể). Khi phản ứng đạt tới trạng thái cân bằng thì áp suất trong bình bằng 0,8 lần áp suất ban đầu khi chưa xảy ra phản ứng ở cùng nhiệt độ. Hằng số cân bằng (KC ) của phản ứng N2 + 3H2 2NH3 xảy ra trong bình là
Câu hỏi số 5:
Cho cân bằng: 2SO2 (k) + O2 (k) ⇄ 2SO3 (k). Khi tăng nhiệt độ thì tỉ khối của hỗn hợp khí so với H2 giảm đi. Phát biểu đúng khi nói về cân bằng này là:
Câu hỏi số 6:
Cho phản ứng: H2 (k) + I2 (k)⇌ 2HI (k) Ở nhiệt độ 430°C, hằng số cân bằng KC của phản ứng trên bằng 53,96. Đun nóng một bình kín dung tích không đổi 10 lít chứa 4,0 gam H2 và 406,4 gam I2. Khi hệ phản ứng đạt trạng thái cân bằng ở 430°C, nồng độ của HI là
Câu hỏi số 7:
Cho cân bằng hoá học của các chất khí A, B, C, D : aA + bB 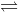 pC +qD. Ở nhiệt độ không đổi, khi áp suất trong bình kín bằng 1,2 at thì tỷ lệ % số mol chất B là 70%. Khi áp suất bằng 3 at thì tỷ lệ % số mol chất B bằng 45%. Nhận xét nào sau đây đúng
pC +qD. Ở nhiệt độ không đổi, khi áp suất trong bình kín bằng 1,2 at thì tỷ lệ % số mol chất B là 70%. Khi áp suất bằng 3 at thì tỷ lệ % số mol chất B bằng 45%. Nhận xét nào sau đây đúng
Câu hỏi số 8:
Axit axetic tác dụng với ancol isopropylic theo phản ứng thuận nghịch: CH3COOH + C3H7OH ⇄ CH3COOC3H7 + H2O Nếu ban đầu người ta cho 1 mol axit axetic tác dụng với 1 mol ancol isopropylic thì cân bằng sẽ đạt được khi có 0,6 mol isopropyl axetat được tạo thành. Lúc đó người ta cho thêm 1 mol axit axetic vào hỗn hợp phản ứng, cân bằng sẽ bị phá vỡ và chuyển dịch đến trạng thái cân bằng mới. Ở trạng thái cân bằng mới, số mol ancol isopropylic là
Câu hỏi số 9:
Cho Ka (CH3COOH) = 1,8.10-5 và Ka (HNO2) = 4,1.10-4. Nếu hai axit có nồng độ mol bằng nhau và ở cùng nhiệt độ thì quá trình điện li đạt tới dạng cân bằng, đánh giá nào sau đây là đúng?
Còn hàng ngàn bài tập hay, nhanh tay thử sức!
>> Luyện thi tốt nghiệp THPT và Đại học, mọi lúc, mọi nơi tất cả các môn cùng các thầy cô giỏi nổi tiếng, dạy hay dễ hiểu trên Tuyensinh247.com.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com









