Cấu tạo nguyên tử - Bảng tuần hoàn
Học bảng tuần hoàn hóa học Mendeleev là một kiến thức quan trọng trong chương trình hóa học phổ thông. Các bạn học sinh đều phải học và ghi nhớ phần
Lưu ý: Chức năng này hiện không còn dùng nữa, vui lòng chọn các khóa học để xem các bài giảng hoặc làm đề thi online!
Bài tập luyện
Câu hỏi số 21:
Dãy nào sau đây gồm các đồng vị của cùng một nguyên tố hóa học?
Câu hỏi số 22:
Cấu hình electron lớp ngoài cùng của nguyên tử kim loại kiềm thổ là
Câu hỏi số 23:
Các nguyên tố từ Li đến F, theo chiều tăng của điện tích hạt nhân thì
Câu hỏi số 24:
Nhận định nào sau đây đúng khi nói về 3 nguyên tử: 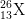 ,
, 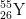 ,
, 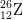 ?
?
Câu hỏi số 25:
Dãy gồm các kim loại đều có cấu tạo mạng tinh thể lập phương tâm khối là:
Câu hỏi số 26:
Trong bảng tuần hoàn các nguyên tố hoá học, nguyên tố X ở nhóm IIA, nguyên tố Y ở nhóm VA. Công thức của hợp chất tạo thành từ 2 nguyên tố trên có dạng là
Câu hỏi số 27:
Trong tự nhiên clo có hai đồng vị bền: 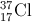 chiếm 24,23% tổng số nguyên tử, còn lại là
chiếm 24,23% tổng số nguyên tử, còn lại là 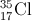 . Thành phần % theo khối lượng của
. Thành phần % theo khối lượng của 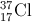 trong HClO4 là
trong HClO4 là
Câu hỏi số 28:
Cấu hình electron của ion Cu2+ và Cr3+ lần lượt là
Câu hỏi số 29:
Phát biểu nào sau đây là sai?
Câu hỏi số 30:
Nguyên tử R tạo được cation R+. Cấu hình electron ở phân lớp ngoài cùng của R+ (ở trạng thái cơ bản) là 2p6. Tổng số hạt mang điện trong nguyên tử R là
Còn hàng ngàn bài tập hay, nhanh tay thử sức!
>> Luyện thi tốt nghiệp THPT và Đại học, mọi lúc, mọi nơi tất cả các môn cùng các thầy cô giỏi nổi tiếng, dạy hay dễ hiểu trên Tuyensinh247.com.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com









